빅파마 경쟁제품 ‘킴리아’·‘예스카타’…안전성·유효성 입증 과제도 남아
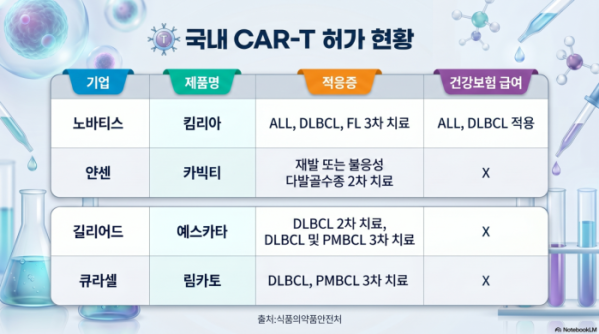
글로벌 빅파마가 선점한 국내 키메릭항원수용체 T세포(CAR-T) 치료제 시장에 국산 기술이 안착할 수 있을지 주목된다. 큐로셀이 국내 기업 가운데 최초로 CAR-T 치료제를 품목허가받으면서 노바티스, 길리어드사이언스와 각축전을 벌일 것으로 보인다. 넓은 적응증을 확보하고, 건강보험 급여권에 진입해 환자 접근성을 강화하는 것이 경쟁에서 살아남는 관건으로 꼽힌다.
3일 제약바이오 업계에 따르면 지난달 29일 식품의약품안전처가 큐로셀이 개발한 CAR-T 치료제 림카토주(성분명 안발캅타젠오토류셀)를 허가하면서 ‘국산 신약 42호’가 탄생했다. 이번 허가는 큐로셀이 2024년 12월 허가를 신청한 이후 약 1년 4개월만의 낭보다. CAR-T 치료제 중에서는 첫 국내 개발 제품으로, 수입 의존도를 완화했다는 점에서 의미가 크다.
림카토는 다른 선택지가 없는 말기 혈액암 환자들의 3차 치료 옵션이 될 것으로 보인다. 적응증은 두 가지 이상의 전신 치료 후 재발하거나 반응하지 않는 미만성 거대 B세포 림프종(DLBCL)과 원발성 종격동 거대 B세포 림프종(PMBCL) 성인 환자다.
그간 국내에는 2017년 노바티스의 ‘킴리아’를 시작으로 2023년 얀센의 ‘카빅티’, 지난해 길리어드사이언스의 ‘예스카타’ 등 3개의 CAR-T 치료제가 품목허가 됐다. 하지만 사실상 환자들의 선택지는 건강보험 급여가 적용되는 킴리아가 유일하다. 예스카타는 올해 1월 진행된 건강보험심사평가원 제1차 암질환심의위원회 심의에서 3차 치료제로 사용 가능한 급여기준을 설정받는 등 급여화 절차를 밟고 있다.
활용 범위 측면에서는 예스카타의 경쟁력이 앞서간다. 예스카타는 1차 화학 면역 요법 치료 이후 12개월 이내에 재발하거나 불응하는 DLBCL 성인 환자 치료 적응증을 확보하고 있어, 일부 환자에서 2차 치료제로 사용할 수 있다. 해당 적응증의 급여화 문제를 차치한다면, 3차 치료제 적응증만 확보한 킴리아와 림카토와 비교해 사용 범위가 넓다. 카빅티 역시 재발 또는 불응성 다발골수종 4차 치료제에서 지난해 2차 치료제로 적응증이 변경됐다.
향후 림카토의 시장 안착은 급여화와 적응증 추가에 달린 것으로 보인다. 림카토는 보건복지부의 허가신청-급여평가-약가협상 병행 시범사업에 선정돼, 식약처의 허가심사와 동시에 건강보험심사평가원 약제급여평가 절차를 진행해 왔다. 허가와 급여 적용 사이의 시간적 격차를 최소화해 빠르게 시장에 진입한다는 전략이다. 큐로셀은 CAR-T 플랫폼에 지속적으로 투자하면서 림카토의 적응증 확대와 글로벌 판로를 모색할 방침이다.
또한 림카토 출시 후 장기적인 모니터링으로 효과를 입증해야 하는 과제도 남았다. 큐로셀은 당초 3상 조건부 허가를 신청했으나, 식약처는 허가 과정에서 3차 요법의 림프종 치료제로 사용되는 신규 CAR-T 제제임을 고려해 3상 임상시험을 면제했다. 대신 시중 CAR-T 치료제와 마찬가지로 허가 후 장기추적조사와 위해성 관리계획을 수립해 안전성과 유효성을 지속적으로 확인하는 조건을 붙였다.
CAR-T 치료는 환자의 면역 T세포를 채취해 암세포를 특이적으로 인식하도록 유전자를 조작한 뒤 환자에게 다시 주입하는 기술이다. 주로 1차 및 2차 치료에 실패한 환자들에게 시도되며, 1회 투여만으로 효과를 기대할 수 있다. 기성 의약품처럼 대량생산할 수 없으며, 공정과 원료 조달 및 유통이 까다롭고 투약 전후 환자 비용이 수억 원에 달한다.
관련 시장도 급성정할 전망이다. 한국바이오협회에 따르면 글로벌 CAR-T 치료제 시장 규모는 2023년 37억4000만달러(약 5조5550억원)를 기록했으며 2029년까지 연평균 39.6% 증가해 290억달러(약 43조원)까지 성장할 것으로 전망된다.