희귀질환 치료 시장 2025년 819조원으로 성장
매년 2월 마지막 날은 세계 희귀질환의 날이다. 유럽 희귀질환기구(EURORDIS)가 4년에 한 번 돌아오는 2월 29일에 착안해 2008년 제정했다.
의약품 개발 기술이 고도화됐음에도 희귀질환 분야에는 여전히 미충족 의료수요가 광범위하다. 글로벌 규제당국은 제도적 인센티브를 강화하며 개발을 독려하고, 제약·바이오업계는 희귀질환을 차세대 성장 동력으로 주목하고 있다.
24일 본지 취재 결과 전 세계적으로 4억명 이상에게 영향을 미치는 7000여건의 희귀질환 가운데 95%는 현재 승인된 치료법이 부재한 것으로 나타났다. 지금까지 수백 종의 치료제가 규제당국의 승인을 받았지만, 대부분의 희귀질환이 아직 질병의 진행을 근본적으로 억제할 수 있는 치료방법이 없다.
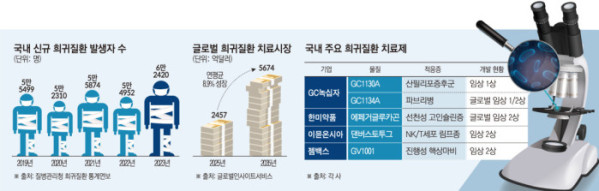
과거에는 희귀질환 치료제의 개발이 활발하지 않은 이유로 상업적 유인 요인이 낮다는 점을 들었지만, 미국과 유럽 등 주요국이 앞다퉈 지원 전략을 확대하면서 이런 우려는 상당 부분 해소됐다. 시장조사기관 글로벌인사이트서비스(Global Insight Services)의 새로운 보고서에 따르면 희귀질환 치료 시장은 2025년 2457억달러(약 355조원) 규모로, 연평균 약 8.9%씩 성장해 2035년 5674억달러(약 819조원)까지 팽창할 것으로 예상된다.
희귀질환 치료제는 대체 치료제가 없는 경우가 많아 1인당 약가가 높게 책정되고, 일정 기간 시장 독점권이 보장돼 가격 경쟁 압력이 제한적이다. 개별 환자의 수는 적지만 수천개의 희귀질환이 존재해 전체 환자군을 합산하면 상당한 수요가 형성되는 점도 시장 확대 요인으로 꼽힌다.
이에 따라 글로벌 기업들은 상업적 성공의 돌파구로 희귀질환 치료제 개발에 매진하고 있다. 미국 식품의약국(FDA)의 희귀의약품 지정(ODD) 건수는 희귀의약품법 제정 이후 첫 10년(1983~1992년)에 비해 최근 10년(2013~2022년) 약 7배 증가했으며, 같은 기간 승인 건수도 6배 늘었다. 그럼에도 전체 희귀질환 중 약 15%만 희귀의약품 지정을 받았고, 실제 치료제는 5%에 불과하단 점에서 기회의 가능성이 크다.
국내에서도 해마다 5만~6만명의 신규 희귀질환자가 발생한다. 질병관리청의 희귀질환자 통계연보에 따르면 국내 희귀질환 신규 발생자는 2023년 6만2420명으로 집계됐다. 특히 진단 기술이 발달하면서 연도별 국내 희귀질환 수는 2019년 926개에서 2023년 1165개로 확대했다.
국내 기업들은 앞다퉈 주요 규제당국의 희귀의약품 지정을 획득하며 치료제 개발에 속도를 내고 있다.
전통 제약사 중 가장 많은 희귀질환 치료제 파이프라인을 가동 중인 GC녹십자는 최근 미국 샌디에이고에서 열린 ‘월드 심포지엄 2026’에서 산필리포증후군 A형 치료제 후보물질 ‘GC1130A’를 선보였다. 2030년 이전에 상용화하는 것이 목표다. 산필리포증후군은 유전적 결함으로 뇌 기능이 손상돼 10~20세에 사망에 이르는 병으로, 소아 약 7만명 당 1명 비율로 발생하는 것으로 알려져 있다.
파프리병 치료제 ‘GC1134A’는 한미약품과 공동 개발하고 있다. 글로벌 임상 1/2상 단계로, 코호트1 대상자 모집을 완료했다.
한미약품이 개발하는 선천성 고인슐린증 치료제 ‘에페거글루카곤’은 이달 초 미국 FDA 혁신치료제(BTD)에 추가 지정됐다. 올해 하반기 글로벌 임상 2상 결과를 발표할 예정이다.
선천성 고인슐린증은 인슐린이 과도하게 분비돼 저혈당증을 유발하는 병으로, 신생아 2만5000~5만명당 1명 꼴로 발병한다. 아직 이를 특정 적응증으로 FDA 승인받은 치료제가 없어 환자들은 췌장 절제에 이른다.
이뮨온시아는 NK/T세포 림프종을 타깃하는 면역항암제 ‘댄버스토투그’의 국내 허가에 속도를 내고 있다. 지난달 식품의약품안전처 ODD 지정을 받으면서 임상 2상만으로 품목허가를 받을 수 있는 길이 열렸다.
NK/T세포 림프종은 국내에서 매년 약 500명 안팎의 신규 환자가 발생하는 희귀암이다. 이뮨온시아는 하반기 글로벌 혁신제품 신속심사(GIFT)를 신청해 2~3년 내 출시하겠단 계획이다.
젬백스는 진행성핵상마비(PSP) 치료제 ‘GV1001’의 국내 임상 2상을 완료하고 글로벌 임상 3상을 준비 중이다. PSP는 파킨슨병과 증상이 일부 유사하지만 진행 속도가 더 빠른 희귀 퇴행성 뇌질환이다. 현재 이를 완치하거나 진행을 완전히 멈추는 약은 없다.
GV1001은 항염증, 항산화, 미토콘드리아 보호 등 다양한 효과를 동시에 나타내는 다중기전 물질이다. 2024년 식약처, 2025년 FDA와 EMA 희귀의약품 지정을 획득해 글로벌 임상시험 시 다양한 혜택 및 지원을 받을 수 있다.
젬백스는 GV1001 저용량을 투여한 PSP 리처드슨 신드롬 유형 환자군에서 질환 진행 속도를 지연시키는 긍정적인 경향성을 확인했다. 또한 선행 임상시험과 연장 임상시험을 합친 72주의 임상시험을 분석한 결과 저용량군에서 외부 대조군 대비 통계적 유의성도 확인했다.
희귀질환 치료제를 개발 중인 기업 관계자는 “희귀질환 치료제는 ‘하이 리스크 하이 리턴(High Risk, High Return)’이란 신약 개발의 산업적 특성이 가장 극명하게 집약된 분야”라며 “최근에는 희귀의약품 지정에 따른 혜택 및 신속심사 제도를 활용하는 등 다양한 인센티브를 제공받을 수 있어 개발 부담이 줄어들고 있다”라고 말했다.





