복지부, '제약산업 육성 및 지원에 관한 특별법' 시행령·시행규칙 및 고시 개정안 입법예고
앞으로 제약기업이 정부로부터 ‘혁신형 제약기업’으로 인증받으려면 매출액 대비 의약품 연구개발비(R&D) 비중을 현행보다 2%포인트(p) 더 높여야 한다.
보건복지부는 이 같은 내용이 포함된 ‘제약산업 육성 및 지원에 관한 특별법(제약산업법)’ 시행령·시행규칙 및 고시 개정안을 입법·행정예고한다고 26일 밝혔다.
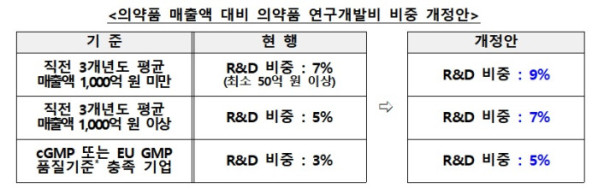
먼저 제약사들의 지속적인 R&D 투자 확대를 유도하기 위해 인증 요건을 상향 조정한다. 현재는 혁신형 제약기업 인증을 받으려면 직전 3개년도 평균 매출액 1000억원 미만 기업은 R&D 비중 7%, 1000억원 이상 기업은 5%를 충족해야 한다. 미국(cGMP)이나 유럽(EU GMP)의 우수 의약품 제조·품질관리 기준을 충족한 기업은 3%의 완화한 기준을 적용받는다.
개정안에 따르면, 매출 1000억 원 미만은 9%, 1000억 원 이상은 7%, cGMP·EU GMP 보유 기업은 5%의 R&D 비중을 달성해야 인증받을 수 있다. 다만 복지부는 제약계의 준비 기간을 고려해 해당 조항의 시행을 공포 후 3년간 유예하기로 했다.
아울러 리베이트 행위에 대한 인증 취소 기준을 개선한다. 기존에는 행정처분에 소송이 제기된 경우 판결 확정일을 처분일로 간주해 수년 전 발생한 위반행위로 뒤늦게 인증이 취소되는 등 기업의 예측 가능성이 떨어진다는 지적이 있었다. 정부는 개정안에서 인증 또는 연장 심사 시점을 기준으로 위반행위 종료 5년이 지났다면 해당 행위를 심사 대상에서 제외하기로 했다. 단 소송이 진행 중인 경우에는 기각 판결일로부터 1년 이내에 인증을 취소할 수 있도록 한다.
이 밖에 혁신형 제약기업을 ‘일반 혁신형’과 ‘외국계 혁신형’으로 구분한다. 외국계 혁신형은 국내 연구·생산시설 유치, 해외자본 유치, 공동연구 등 항목 배점이 확대되고, 본사에 권한이 집중된 비임상·임상시험 후보물질 개발이나 특허 기술이전 성과 등 배점은 축소된다. 외국계 제약사는 일반 혁신형과 외국계 혁신형 중 유리한 쪽을 선택해 신청할 수 있다.
복지부는 행정예고 기간 국민 의견을 수렴해 개정안을 확정할 방침이다. 또 올해 중 ‘국가 제약바이오산업 육성 전략’을 별도 수립할 계획이다.





