국내 제약·바이오기업들이 연내 신종 코로나바이러스 감염증(코로나19) 치료제 개발, 내년 백신 사용을 목표로 숨가쁘게 달리고 있다. 글로벌 제약사들과 비교해도 크게 뒤처지지 않는 속도다. 전 세계 코로나19 확진자 수가 5000만 명에 육박한 가운데 우리나라가 '조기 종식'의 꿈을 이룰 수 있을지 주목된다.
4일 식품의약품안전처에 따르면 코로나19 치료제·백신 관련 임상에 진입한 국내 제약·바이오기업은 총 10곳이다. 식약처가 전날 바이오기업 뉴젠테라퓨틱스가 개발하는 '뉴젠나파모스타트정'의 임상 1상을 승인하면서 국내 기업이 임상 중인 코로나19 치료제는 총 11종으로 늘었다. 백신은 제넥신의 'GX-19'가 임상을 진행하고 있다.
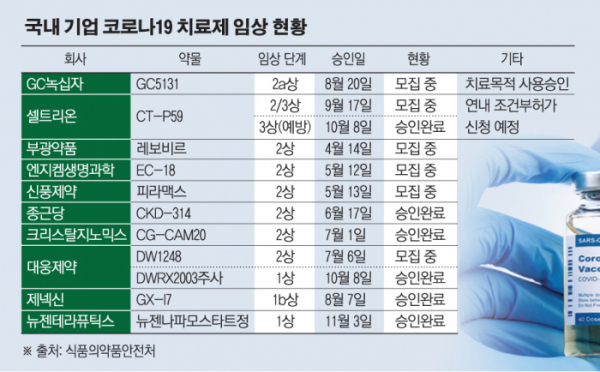
GC녹십자는 의료기관에서 GC5131A의 사용 사례가 늘어나면서 생산량 증대에 돌입했다. 이미 240ℓ의 혈장을 투입해 2차 생산을 완료한 회사는 동일한 규모의 3차 생산을 통해 차질없이 혈장치료제를 공급할 계획이다. 이와 함께 임상 2상을 진행하는 의료기관 6곳을 추가 확보, 임상에 속도를 내고 있다.
업계는 혈장치료제의 임상이 순조롭게 진행되면서 목표대로 연내 개발이 가능할 것으로 내다보고 있다. 다만, 혈장치료제는 완치자의 혈장이 필요하다는 점에서 대량 생산에는 한계가 있다.
셀트리온은 코로나19 항체치료제 'CT-P59'의 임상 2/3상과 예방임상 3상을 동시 진행 중이다. 예방임상은 밀접 접촉자 및 무증상 확진자를 대상으로 진행하는 것으로, 성공하면 의료진이나 면역력이 취약한 고연령층 등 코로나19 고위험군에 예방 목적으로 쓰일 수 있다.
경증·중등증 환자를 대상으로 하는 임상 2/3상은 연말까지 중간 결과를 확보할 계획이다. 이 결과에 따라 조건부 허가가 가능해진다. 서정진 셀트리온그룹 회장은 직접 올해 안에 조건부허가를 신청하겠다고 언급한 바 있다.
최근 미국에서는 일라이릴리와 리제네론이 연달아 중증 환자를 대상으로 진행 중인 항체치료제의 임상을 중단했다. 치료효과보다 안전성이 더 우려된다고 판단됐기 때문이다. 이들은 미국 식품의약국(FDA)에 각각 항체치료제의 긴급사용승인(EAU)을 신청한 바 있다. 리제네론의 항체치료제는 도널드 트럼프 미국 대통령이 투여 후 "즉시 상태가 좋아졌다"고 극찬했던 약물이기도 하다.
전 세계적으로 주목받던 항체치료제들이 임상에 차질을 빚으면서 CT-P59에 대한 관심도 높아지고 있다. 셀트리온 관계자는 "현재까지 임상이 순조롭게 진행되고 있다"면서 "연내 조건부허가를 신청하겠다는 계획대로 가는 중"이라고 말했다.
이밖에도 국내에서 코로나19 치료제 임상 승인을 받은 기업은 부광약품, 엔지켐생명과학, 신풍제약, 종근당, 크리스탈지노믹스, 대웅제약, 제넥신이 있다. 이 가운데 환자 투여를 진행 중인 곳은 부광약품, 엔지켐생명과학, 신풍제약, 대웅제약 등 4곳이다.
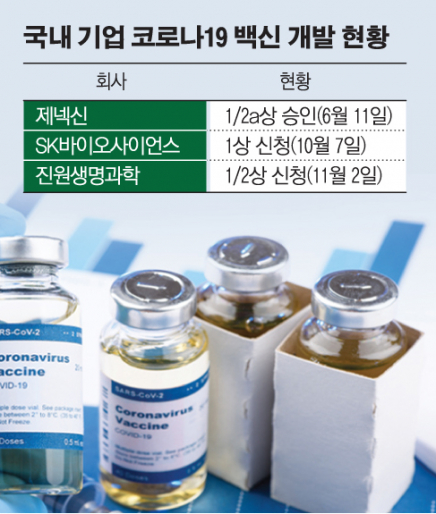
코로나19 백신 임상을 진행 중인 국내 기업은 제넥신이 유일하다. 제넥신이 산·학·연 컨소시엄을 구성해 개발 중인 코로나19 백신 'GX-19' 지난 6월 11일 1/2a상 승인을 받았다. 이달 중 임상 2a상에 들어가는 것이 목표다.
제넥신은 GX-19의 대량생산 타당성을 검토하기 위해 연간 2만ℓ 규모의 위탁생산(CMO) 시설 완공을 앞둔 폴루스와 양해각서(MOU)를 체결했다. 2b/3상을 위한 시료 생산과 공정 개발도 서두르고 있다. 특히 인도네시아와 태국 등 해외 파트너사를 통해 대규모 글로벌 임상 2상을 진행, 개발 속도를 당길 예정이다. 임상 2상 결과에 따라 내년 여름께 환자에 사용할 수 있을 것으로 회사 측은 기대하고 있다.
글로벌 제약사들도 코로나19 백신 상용화를 서두르고 있다. 미국의 모더나는 이달 말께 1만5000명을 대상으로 한 임상 3상 결과를 내놓고, 미국 FDA에 승인을 신청할 예정이다. 내년 봄부터 백신의 유통이 가능할 것으로 전망된다. 화이자와 바이오엔텍도 FDA 승인 신청을 앞두고 있다. 계획대로 승인된다면 국산 백신과의 격차는 약 6개월 정도로 예상된다.
SK바이오사이언스와 진원생명과학은 각각 식약처에 임상시험계획(IND)를 제출한 상태다. 정부는 이들 기업이 연내 임상 1상에 진입할 것이라 공언했다.
진원생명과학의 'GLS-5310'은 GX-19와 마찬가지로 DNA 백신이다. 예방효능을 높이기 위해 코로나19 바이러스 표면에 있는 스파이크 단백질 항원 이외에 1개의 항원이 추가된 것이 특징이다.





