희귀질환 치료제 개발은 각국 규제당국의 정책적 판단이 성패를 가르는 영역으로 자리잡았다. 미국과 유럽 등 주요 국가들은 법·제도 정비는 물론 신속심사, 조건부허가, 연구비 지원까지 동원하며 개발 장벽을 낮추는 데 주력하고 있다.
24일 본지 취재 결과 희귀질환 치료제 개발을 가장 적극적으로 장려하는 국가는 세계 최대 의약품 시장 미국이다. 미국은 1983년 희귀의약품법을 제정, 다른 국가의 움직임을 촉진해 연구개발(R&D) 환경을 크게 개선시켰다. 실제로 일본(1993년), 호주(1997년), 유럽연합(1999년), 스위스(2000년), 한국(2003년)에서 법률이 제정됐다.
미국 식품의약국(FDA)은 패스트트랙, 가속승인, 우선심사 등 다양한 신속심사 프로그램을 운영해 혁신적인 치료제가 환자들에게 최대한 빨리 도달하도록 노력하고 있다. 임상 근거에 유연성을 적용해 치료 효능을 합리적으로 예측할 수 있는 대리 지표를 승인에 활용하면서 극히 적은 환자 집단을 대상으로 임상 연구를 설계하고 수행해야 하는 희귀질환 치료제 개발의 숨통을 틔웠다.
자금 지원도 동반된다. 미국 국립보건원(NIH)은 지난해 희귀질환 임상연구 네트워크에 약 2600만 달러(약 375억원)를 지원해 학계와 산업계 간의 협력을 증진하고 R&D를 강화했다.
유럽의약품청(EMA) 역시 가속평가, 조건부허가 등의 제도를 운영 중이다. 또한 ‘클러스터’라 불리는 협력 그룹을 가동해 희귀의약품 지정과 제품 개발, 행정 절차 간소화를 논의한다.
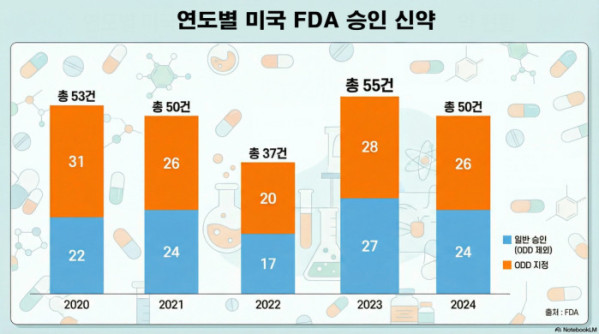
이런 노력의 결과 현재 희귀질환 치료제는 FDA와 EMA가 승인한 신약의 약 50%를 차지한다. 특히 FDA 승인 치료제 가운데 희귀의약품 지정(ODD)은 물론 패스트트랙까지 동시 획득한 사례는 2020년 11건, 2021년 9건, 2022년 13건, 2023년 13건 등 해마다 전체 승인 건수의 20%를 넘는다.
국내에서도 희귀의약품 지정 기준을 대폭 완화하는 등 지원을 강화하고 있다. 지난해 12월 식품의약품안전처가 ‘희귀의약품 지정에 관한 규정’을 개정하면서 희귀질환 치료·진단이 목적인 의약품은 ‘대체의약품 대비 안전성·유효성 개선 입증 자료’ 없이도 희귀의약품에 신속하게 지정받을 수 있게 됐다. 유병인구 2만명 이하 또는 진단이 어려워 환자 규모 파악이 불가능한 질환이 기준이다.
이에 앞서 식약처는 글로벌 혁신제품 신속심사 지원체계(Global Innovative products on Fast Track, GIFT)를 도입, 근무일 기준 120일의 일반심사기간을 90일로 25% 단축시켰다. 아울러 준비된 자료부터 먼저 심사하는 수시 동반심사를 적용하고, 안전에 직접 관련 없는 일부 자료는 시판 후 제출할 수 있는 근거 규정을 적용하고 있다.
2022년 GIFT 도입 이후 3년간 39개 품목이 허가됐으며, 그중 85%는 중증근무력증, 소아 신경모세포종, 재발·난치암 치료제 등 희귀·중증질환 의약품으로 나타났다. 허가 품목 중 46%는 기존 대체 치료제가 전무했던 약물로, 미충족 의료 수요 해소에 직접 기여했다는 평가다.





