메지온의 발기부전증치료제 유데나필 관련 미국 FDA 회의를 성공적으로 마쳐 ‘최종허가까지 문제 없을 것’이라는 자신감을 드러냈다.
10일 메지온에 따르면 유데나필의 발기부전증치료제 관련 FDA Mid-Cycle Review 회의를 한국시간으로 9일 밤에 성공적으로 마무리 했다.
Mid-Cycle Review는 제약회사가 NDA(신약허가신청)를 제출하면 최종허가 전에 하는 FDA 미팅 중 하나로 신청된 자료들을 중간 검토하는 회의라 할 수 있다.
만일 이 회의에서 문제가 생길 경우 Advisory Committee를 통해 외부 전문가들의 객관적인 의견을 전달 받지만, 유데나필은 이 과정을 거치지 않고 진행하기로 FDA에서 통보받았다.
유데나필은 9월에 있을 최종 점검 회의인 Late Cycle Review를 통과하면 내년 1월 최종 허가를 받는 과정은 순항할 것으로 예상했다.
메지온 관계자는 “올 가을에 있을 회의도 잘 준비하여 내년 1월에 있을 최종허가까지 문제없도록 할 것” 이라고 강조했다.
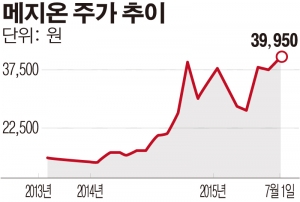
주식시장에서는 슈넬생명과학, 씨젠, 파미셀, 한미사이언스 등 바이오 관련 기업들에 대한 기대감이 높은 상황에서 메지온의 FDA 허가 진행이 순항하면서 관심이 모아지고 있다.