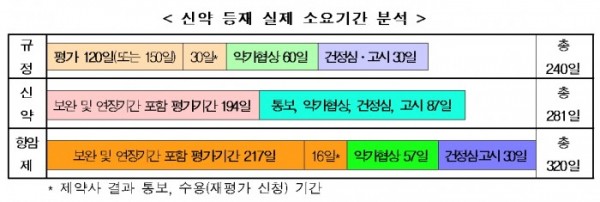
현재, 관련 규정상 신약의 등재기간은 신청 후 약 240일(또는 270일)이며, 평가기간 중 자료에 대한 보완 요청(회당 14일)과 제약사의 평가기간 연장 요청(총 90일) 기간은 포함되지 않는다.
복지부와 심평원은 2011~2015년에 등재된 신약(132성분), 항암신약(19성분)의 신약 등재 절차 시간을 분석한 결과 전체 신약은 신청부터 등재까지 평균 281일이 소요됐고, 항암신약은 신청 후 평가완료일까지 217일, 이후 기간 103일(제약사 결과수용, 약가협상ㆍ고시) 등 평균 약 320일이 소요된 것으로 나타났다.
특히, 선별등재 제도 하에서 항암신약 등은 비용효과성 검토를 위한 자료 보완, 평가기간 연장 등으로 인해 상당 시일이 소요되는 것으로 분석됐다.
신약 등재 절차는 제약사가 급여적정성 평가를 신청하면 심평원이 급여적정성 평가를 한 후, 건보공단 약가 협상을 거친 뒤 복지부 건정심 심의와 복지부 장관 고시로 진행된다.
항암신약의 경우 대부분 고가로 제출된 경제성평가 자료의 면밀한 검토가 필요하며, 이 과정에서 제약사가 신청가격을 조정하거나 효과 추정에 대한 근거자료 보완 등이 다수 발생하고 있다.
이에 따라, 복지부와 심평원은 제약사의 완결성 높은 등재 신청을 지원해 자료 보완 등에 소요되는 기간을 줄여나가기로 했다.
먼저 심평원 내 신약 등재신청 제출자료 '사전 평가지원팀'을 구성하고 평가자료의 사전 컨설팅 등을 실시키로 했다.
지원팀에서 제약사 제출 내용을 사전 검토ㆍ확인 후 미비시 대면 상담(컨설팅)을 실시하고 필요한 자료를 구비하도록 안내한다.
제약사의 평가신청이 용이하도록 '다빈도 보완요청 유형 사례집'과 '표준 참조 사례(reference case)'를 배포할 예정이다.
또 제약사 약가 관련 담당자 대상 주기적 교육을 제공할 계획이다. 심평원이 반기 또는 분기별로 제약사 대상 교육 프로그램을 운영한다.
'사전 평가지원팀'은 관련 전문 인력 보강 등을 통해 9월부터 구성ㆍ운영하고, 조속히 사전 평가지원 체계를 확립해 교육을 실시한다.
한편, 글로벌 혁신신약의 심평원 평가 기간과 건보공단 협상 기간 등 규정 상의 등재기간 단축도 병행 추진한다. 항암제 등의 보험평가와 약가협상 연계를 통해 실제 소요기간을 줄여나갈 방침이다.
아울러 국내 보건의료 발전에 기여한 양질 의약품이 조속히 등재될 수 있도록, 10월부터 글로벌 혁신신약은 100일 이내에 평가하고 30일 이내 협상(현재 60일)을 실시할 예정이다.





