HLB가 개발한 담관암 신약의 미국 식품의약국(FDA) 우선심사 여부가 조만간 판가름난다. 간암에 이어 담관암까지 도전을 이어온 HLB가 FDA 허가 신약을 탄생시키겠다는 오랜 목표를 현실화할 수 있을지 주목된다.
23일 본지 취재를 종합하면 미국 FDA는 이달 27일(현지시간)까지 HLB의 미국 자회사 엘레바테라퓨틱스가 신약허가(NDA)를 신청한 FGFR2 융합·재배열 표적항암제 ‘리라푸그라티닙’의 우선심사 여부를 결정한다. 우선심사 품목으로 지정되면 심사 기간이 6개월로 단축돼 9월 말까지 허가 여부가 드러난다. 일반심사가 적용될 경우엔 약 10개월이 소요된다.
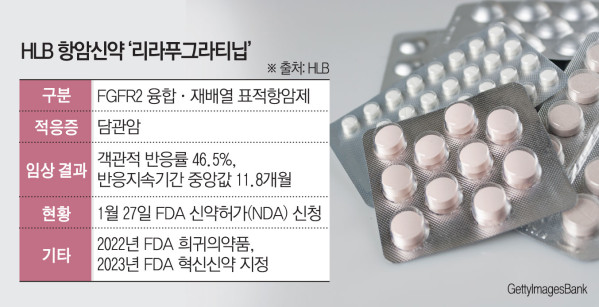
리라푸그라티닙은 2022년 FDA 희귀의약품, 2023년 혁신신약에 지정돼 임상 2상 결과만으로 가속승인 절차를 밟고 있다. 담관암 임상 2상(ReFocus)에서 기존 2차치료제 허가 약물 대비 가장 높은 객관적 반응률(ORR, 46.5%)과 반응지속기간 중앙값(mDOR, 11.8개월)을 확인했다. 안전성 측면에서도 이상반응은 전반적으로 예측할 수 있고 관리 가능한 수준이며, 범FGFR 억제제의 주요 부작용으로 알려진 고인산혈증과 설사 발생률은 각각 20.7%, 21.6%로 기존 허가 약물보다 낮다. 효능과 안전성 측면에서 ‘계열 내 최고(Best-in-Class)’ 치료제의 경쟁력을 입증했다는 것이 회사 측의 설명이다.
FGFR2는 ‘섬유아세포 성장인자 수용체 2(Fibroblast Growth Factor Receptor 2)’로 세포 표면에서 성장 신호를 전달하는 단백질이다. 정상 상태에서는 조직 발달과 손상 회복 등 필요한 상황에서만 제한적으로 활성화되지만, 변이 또는 재배열이 발생하면 신호 체계가 비정상적으로 활성화되면서 세포 증식이 통제되지 않는 상태로 이어진다. 특히 담관암에서는 FGFR2 재배열이 비교적 높은 빈도로 관찰되는 것으로 알려져 있다.
담관암은 간과 담낭, 소장을 연결하는 담관에서 발생하는 악성 종양으로, 진행 속도가 빠르고 예후가 나빠 대표적인 난치암으로 꼽힌다. 초기 증상이 거의 없어 상당수 환자가 진행성 단계에서 진단되는 경우가 많다. 미국에서는 연간 약 8000명의 신규 환자가 발생하는 것으로 보고된다.
HLB는 간암 신약(리보세라닙+캄렐리주맙)의 미국 허가를 추진 중이지만, FDA로부터 두 차례에 걸쳐 보완요구서를 받으면서 승인이 지연되고 있다. 그사이 리라푸그라티닙의 개발에 박차를 가해 올해 1월 간암 신약 허가 재신청과 담관암 신약 허가 신청을 나란히 제출했다. 회사 관계자는 “우선심사로 가면 올해 9월, 일반심사라면 내년 리라푸그라티닙의 허가 여부가 결정된다”라면서 “FDA의 선택에 맞춰 차질없이 절차를 진행해 가겠다”라고 말했다.
엘레바는 다음 달 17일부터 22일까지 미국 샌디에이고에서 열리는 미국암연구학회 연례학술대회(AACR 2026)에서 리라푸그라티닙을 기존 범FGFR 저해제와 비교한 분석 결과를 공개한다. 해당 결과는 상업화 과정에서 차별성을 강조하는 근거로 활용될 전망이다.





