바이오니아의 자회사 써나젠테라퓨틱스는 리보핵산 간섭(RNAi) 기반 항섬유화 신약 ‘SRN-001’의 임상 1a상 보고서를 통해 긍정적인 결과를 확인했다고 20일 밝혔다. 이 결과는 향후 임상 시험 최종 결과 보고서(CSR)를 통해 공식적으로 발표될 예정이다.
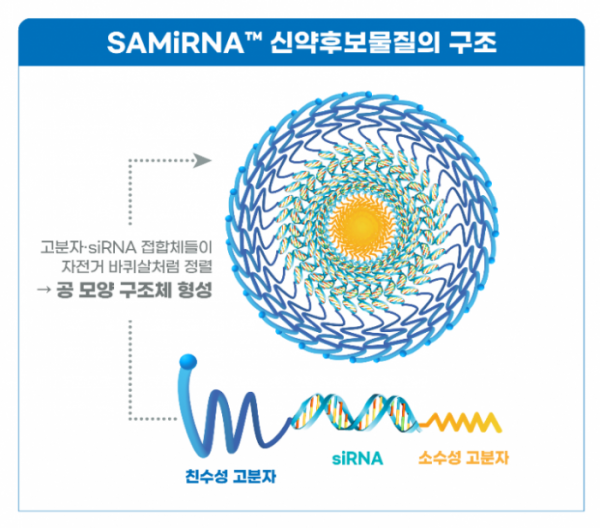
써나젠은 지난해 9월 기존 RNAi 치료제의 문제점인 체내 투여 시 쉽게 분해돼 병소까지 전달이 어렵고 선천 면역 염증 반응을 일으키는 문제를 해결한 초분자 RNAi 나노 구조체 SAMiRNA™ 기반의 항섬유화 신약 SRN-001의 호주 임상 1a상을 진행해왔다.
보고서에 따르면 SRN-001은 인체에서 충분한 안전성과 내약성을 확인했다. 이번 임상은 SAMiRNA 플랫폼을 적용한 짧은 간섭 리보핵산(siRNA)이 인간에게 전신 투여로 연구된 첫 번째 사례로 건강한 피험자를 대상의 단일 용량 연구였다.
연구 결과 질병 마우스 모델에서 효과적인 용량의 인체 등가 용량보다 약 10배 높은 최대 용량에서도 용량 제한 부작용이 관찰되지 않아 높은 수준의 내약성을 확인했다. 또 약동학(PK) 결과에서도 투여 용량에 비례해 노출도가 상관관계가 있음을 확인하는 등 임상 1a상을 성공적으로 완료했다.
특발성 폐섬유증(IPF)은 폐에 콜라겐이 비정상적으로 축적돼 폐 기능을 상실하게 하는 난치병으로, 진단 후 5년 생존율이 40%에 불과하다. 글로벌 시장조사기관 리서치앤드마켓에 따르면 특발성 폐섬유증 치료제 시장 규모는 2030년까지 61억 달러(약 8조4000억 원)에 이를 것으로 전망된다.
회사는 SRN-001이 섬유증 유발 mRNA를 분해해 근본적인 치료가 가능할 것으로 기대되며, 시장의 판도를 바꿀 수 있는 잠재력을 기대하고 있다.
박준영 써나젠테라퓨틱스 대표는 “SAMiRNA 플랫폼의 첫 번째 인간 대상 연구를 성공적으로 완료한 것에 대해 기쁘게 생각한다”며 “향후 전략적 파트너십을 통해 개발의 다음 단계로 나아가고, 이와 같은 잠재적으로 질병을 수정할 수 있는 치료법이 있어야 하는 환자들에게 제공할 수 있기를 기대한다"고 덧붙였다.





