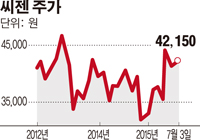
[종목돋보기] 분자진단업체 씨젠이 호흡기질환 관련 신제품 2종을 이달 중순 판매할 예정이다. 씨젠 측은 이를 위해 유럽 인증을 완료했으며 향후 미국 FDA(식품의약국) 인허가 획득에도 나선다는 방침이다.
3일 씨젠은 호환이 가능한 신개념의 MuDT 분자진단 기술을 적용한 신제품들을 지난해 말과 올해 5월에 출시한데 이어 이달 중순 추가로 출시한다고 밝혔다.
이번에 출시되는 신제품 2종은 제품은 올플렉스(Allplex™) 신제품군에 속하는 제품으로 경쟁사 제품 대비 저렴한 비용으로 한번에 다수의 질병 원인 병원체를 간편하게 검사할 수 있는 차세대 제품으로 각광받고 있는 제품이다.
올플렉스(Allplex™) 신제품군은 차세대 Real-time PCR 기술인 MuDT™기술 기반으로 하는 제품으로 소화기, 호흡기, 성감염증 등 총 3가지 제품군, 12개 제품으로 이뤄졌다.
호흡기 질환 관련 제품의 경우 지난해 2종이 먼저 출시된 바 있으며 올해 5월에는 소화기 관련 제품들이 출시됐다. 성감염증 관련 제품의 경우 내년 상반기 출시 예정인 것으로 알려졌다.
씨젠 관계자는 "올해 출시된 제품의 경우 출시 전 진행된 사전 평가에서 긍정적인 평가를 받으면서 현재 주문이 들어오고 있는 상황"이라며 "연이은 신제품 출시로 매출 성장이 기대된다"고 밝혔다.
특히 씨젠은 최근 출시한 신제품들을 통해 미국 시장 진출을 꾀하고 있다. 회사 측 관계자는 "분자진단시장의 경우 현재 미국이 가장 크다"며 "미국 시장 진출을 위해 현재 미국 FDA 인허가 획득을 추진 중에 있다"고 강조했다.
이어 "올해 초 헤르페스바이러스(HSV) 유전자 증폭시약에 대한 미국 식품의약청(FDA)의 의료기기 허가를 받았으나 이 제품의 경우 씨젠의 주요제품은 아니다"며 "씨젠은 향후 차세대 신제품을 통한 본격적인 미국 시장 진출에 나설 것"이라고 밝혔다.
씨젠은 현재 이를 위한 사전 준비 작업에 돌입한 상태로 이르면 오는 2018년, 이르면 2017년까지는 미국 FDA 인허가 획득에 나설 수 있을 것으로 기대하고 있다.
☞ 투자자 300명에게 공개하는 종목의 속살 이투데이 스탁프리미엄에서 확인하세요





