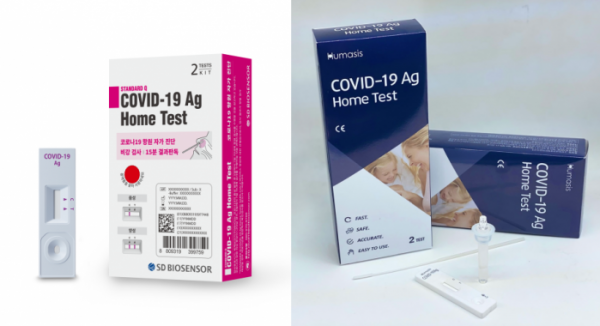
셀트리온은 체외진단 전문기업 휴마시스와 공동개발한 코로나19 현장형 항원신속진단키트 '디아트러스트(Celltrion DiaTrust COVID-19 Ag Rapid Test)' 가 미국 식품의약국(FDA)의 긴급사용승인을 획득했다고 19일 밝혔다. 지난해 12월 미국 자회사 셀트리온USA를 통해 미국 뉴욕에 있는 진단키트 및 개인보호장비 전문 도매유통사 '프라임 헬스케어 디스트리뷰터스'와 2400억 원 규모의 코로나19 항원진단키트 공급 계약을 체결한 만큼 디아트러스트를 즉시 공급할 예정이다.
디아트러스트는 코로나19에 특이적으로 강하게 결합하는 셀트리온 개발 항체를 적용해 바이러스의 항원을 인식하는 제품으로, 감염 여부를 15분 이내에 진단할 수 있다. 일반적으로 N항원이나 S항원 중 하나만 검출하는 경쟁사의 신속진단키트와 달리 두 항원 모두를 검출하는 ‘듀얼항원’ 방식으로 민감도를 극대화한 것이 특징이다. 코로나19 초기 증상자 대상 임상시험에서 민감도와 특이도에서 각각 93.3%, 99.1%의 결과를 보였다.
지엘라파는 한국코러스와 주도하는 러시아의 코로나19 백신 '스푸트니크V' 컨소시엄에서 휴메딕스를 배제한다고 19일 밝혔다. 앞서 지엘라파와 자회사 한국코러스는 스푸트니크V의 개발을 지원한 러시아 국부펀드(RDIF)와 국내 위탁생산에 합의하고, 바이넥스, 보령바이오파마, 이수앱지스, 종근당바이오, 큐라티스, 휴메딕스, 안동 동물세포실증지원센터와 스푸트니크V 생산을 위한 컨소시엄을 구성한 바 있다.
한국코러스 관계자는 "스푸트니크V 생산을 위해 컨소시엄 업체들과 중요 정보들을 공유하며 협의를 진행하고 있는 상황에서 휴메딕스가 어떤 상의도 없이 다른 컨소시엄에 참여하는 행위는 상호 간의 신의를 저버린 행위"라며 "도의상 있을 수 없는 일이라고 판단해 지엘라파와 한국코러스가 주도하는 컨소시엄에서는 휴메딕스를 배제하기로 했다"고 설명했다.
유바이오로직스는 필리핀 제약사 글로백스(Glovax Biotech)와 개발 중인 코로나19 백신 '유코백-19' 기술이전에 대한 의향서(LOI)를 체결했다고 19일 밝혔다. 필리핀 정부가 추진 중인 백신 제조 공장에 유코백-19 백신에 대한 항원생산 관련 원천기술, 완제품 생산기술 및 GMP 운영에 대한 노하우를 글로백스에 이전할 예정이다.
글로백스는 유코백-19를 현지에 조속하게 공급하기 위해 유바이오로직스와 함께 임상2상을 추진하고 있다. 임상2상 종료 후 긴급사용 승인을 통해 현지에 유코백-19를 공급할 예정이다.
한국비엔씨는 대만 골든바이오텍의 공식 통보를 통해 미국 FDA 승인을 받은 코로나19 치료후보 물질 안트로퀴노놀을 이용한 2상 임상시험에서 80명에 대한 피험자 등록을 마쳤다고 19일 밝혔다. 임상 2상 시험의 2단계 결과가 최종 확인된 후 2차 외부독립위원회(DMC) 회의를 소집해 중간 결과 분석을 진행하고 이를 확인할 예정이다.
한국비엔씨는 임상 2상 결과가 성공적이면 FDA에 긴급사용승인을 신청할 계획이다. 이 회사는 한국, 러시아, 터키, 우크라이나에 대한 안트로퀴노놀의 독점 제조와 판매권리를 확보했다.
에이치엘비생명과학은 진행성 또는 전이성 위암 및 위식도접합부암 환자를 대상으로 리보세라닙 병용요법을 1차 치료제로 개발하기 위한 임상시험계획(IND)을 식품의약품안전처에 제출했다고 19일 공시했다. 이번 임상은 이전 치료력이 없는 위암 환자 총 885명을 대상으로 캄렐리주맙과 카페시타빈/옥살리플라틴을 병용투여 후 캄렐리주맙과 리보세라닙을 병용투여한 354명의 치료결과를 대조군인 카페시타빈/옥살리플리틴 병용투여군 354명, 캄렐리주맙과 카페시타빈/옥살리플라틴 병용투여 후 캄렐리주맙 단독투여군 177명의 치료결과와 비교하는 방식으로 진행된다.
리보세라닙은 현재 에이치엘비가 말기 위암에 대해 미국 식품의약국(FDA)에 신약허가신청(NDA) 제출을 준비하고 있다. 위암 2차 치료제로 파클리탁셀과 병용 임상 2상도 진행 중이다.
한미약품은 파트너사인 사노피가 '아모잘탄큐'의 현지 제품명인 '트리스타니움'으로 러시아 연방 보건부(MOH, Ministy of Health of the Russian Federation)의 시판허가를 받았다고 20일 밝혔다. 아모잘탄큐는 CCB계열 고혈압치료성분 암로디핀캄실산염과 ARB계열 고혈압치료성분 로사르탄에 고지혈증치료제 로수바스타틴을 결합한 3제 복합신약이다.
한미약품은 사노피에 아모잘탄큐의 러시아 독점 허가자료 사용권을 제공하고, 사노피는 러시아 현지 허가, 영업 및 마케팅, 판매를 전담한다. 사노피는 이번에 시판허가를 획득해 판매 전략 및 마케팅 전략 등을 수립한 후 공식 발매에 나설 계획이다. 한미약품은 경기도 팔탄 스마트플랜트에서 완제품을 생산해 러시아 현지로 수출한다.
휴온스랩은 프롤리아 바이오시밀러 개발을 위해 팬젠과 세포주 및 생산 기술 도입 계약을 체결했다고 20일 밝혔다. 팬젠이 개발 중인 골다공증 및 암환자 골소실 치료용 항체 치료제 프롤리아의 바이오시밀러 '데노수맙(Denosumab)' 생산을 위한 세포주와 배양 및 정제 공정 기술을 이전받아 본격 개발에 착수한다.
프롤리아는 뼈를 파괴하는 파골세포에 필수적인 단백질 RANKL과 결합해 파골세포의 형성, 기능, 생존을 억제해 골파괴에 이르는 악순환을 방지해주는 약물이다. 지난해 글로벌 매출 약 5조7000억 원(51억 달러)을 기록했다.
식약처는 '의약품 GMP 특별 기획점검단'의 의약품 제조업체 특별 불시 점검 결과 약사법 위반 사례가 확인된 종근당에 대해 잠정 제조‧판매 중지 등 조치했다고 21일 밝혔다. 이번 점검을 통해 식약처는 △변경허가를 받지 않고 첨가제 임의 사용 △제조기록서 거짓 이중작성·폐기 △제조방법 미변경 △원료 사용량 임의 증감 등 약사법 위반 사항을 확인해 종근당에서 제조(수탁제조 포함)한 9개 의약품에 대해 잠정 제조‧판매를 중지했다.
이와 관련해 한국제약바이오협회는 오는 27일 오후 윤리위원회를 개최할 예정이다.
씨젠은 영국 스코틀랜드에 약 1600만 파운드(약 247억 원) 규모의 코로나19 진단키트를 공급한다고 22일 밝혔다. 이번 공급은 코로나19 유행 이후 스코틀랜드 정부가 진행한 코로나19 진단시약 입찰로는 가장 큰 규모다.
스코틀랜드에 공급되는 씨젠의 코로나19 진단키트(Allplex SARS-CoV-2 Assay)는 지난해 6월 유럽 CE 인증 및 12월 식약처 정식 허가를 받았다. 코로나19 바이러스 유전자 겨냥 4개(E, RdRP, N, S gene)와 핵산 추출부터 PCR까지 전 과정 검사 유효성 검증 유전자(Exo IC)까지 총 5개의 유전자를 겨냥해 한 번의 검사로 진단할 수 있는 멀티플렉스 진단 제품이다.
프레스티지바이오파마는 러시아 제약사 파마파크와 함께 '아바스틴'의 바이오시밀러 'HD204'의 러시아 진출을 추진한다고 23일 밝혔다. HD204의 상용화를 위한 이번 라이선스 계약에 따라 파마파크는 러시아 내 HD204의 판매 및 상업화를 독점적으로 주도한다. 프레스티지바이오파마는 한국 오송에 있는 관계사 프레스티지바이오로직스를 통해 제품을 제조할 예정이다.
HD204는 현재 글로벌 임상 3상을 진행 중이다. 아바스틴과의 약동학 및 면역원성, 안전성 비교를 위해 호주에서 진행했던 임상 1상에서 미국 및 유럽산 원약과의 동등성을 입증한 바 있다.
식약처는 코로나19 자가검사가 가능한 에스디바이오센서와 휴마시스의 항원방식 자가검사키트 제품에 대해 추후 자가검사에 대한 추가 임상적 성능시험 자료 등을 3개월 내에 제출하는 조건으로 23일 품목허가했다. 이번에 허가한 2개의 제품은 국내에서 전문가용으로 허가를 받았으며, 해외에서는 자가검사용 임상시험을 실시해 긴급사용승인 등을 받은 바 있다.
에스디바이오센서 제품은 지난해 11월 식약처에서 임상적 민감도 90%(54/60명), 특이도 96%(96/100명)로 전문가용 제조품목 허가를 받아 독일, 네덜란드, 덴마크, 스위스, 포르투칼, 룩셈부르크, 체코 등 7개국에서 자가검사용으로 사용 중이다. 휴마시스 제품은 지난달 식약처에 임상적 민감도 89.4%(59/66명), 특이도 100%(160/160명)로 전문가용 허가를 받고 체코, 덴마크, 오스트리아 등 3개국에서 자가검사용으로 사용되고 있다.
한국코러스는 러시아의 코로나19 백신 '스푸트니크V'가 국내에서 사용될 때를 대비해 대·내외적 준비를 진행 중이라고 23일 밝혔다. 국내 사용 승인에 필요한 서류를 러시아 국부펀드(RDIF)에 요청해 RDIF에서 해당 서류를 준비하고 있으며, 기타 필요 사항에 대해 허가당국에 요건을 확인 중이다.
스푸트니크V는 밸리데이션 배치 물량이 러시아로 보내져 상업 생산 물량 출하를 앞두고 있다. 한국코러스는 해당 밸리데이션 배치를 RDIF 및 가말레야 연구소 기술진과 함께 춘천공장에서 생산하고 수율과 품질이 기준치를 충족하는 것을 확인했다.









![키키도 소환한 그 감성⋯Y2K, 왜 아직도 먹히냐면요 [솔드아웃]](https://img.etoday.co.kr/crop/320/200/2292619.jpg)