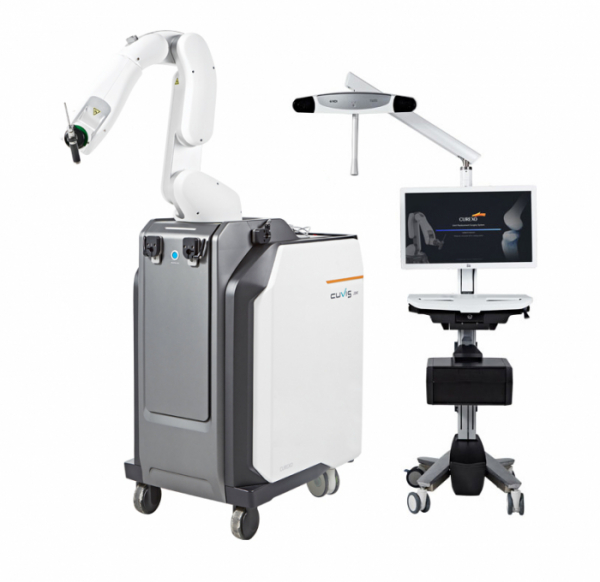
의료로봇·재활로봇 생산 및 의료솔루션 기업 큐렉소가 올해 하반기 내 미국 식품의약국(FDA)에 인공관절 수술로봇(큐비스 조인트, Cuvis Joint)의 허가 신청서를 제출한다.
2일 회사와 의료기기업계에 따르면 큐렉소는 지난해 6월 식품의약품안전처(KFDA)로부터 판매 승인을 받은 큐비스 조인트의 미국 허가를 위한 막바지 작업을 준비 중이며 늦어도 4분기 이내에 신청서를 전달할 계획이다.
큐렉소 관계자는 “큐비스 조인트의 미국 FDA 허가 신청은 유럽 CE 승인을 받는 대로 진행할 예정”이라며 “내부에선 4분기쯤으로 보고 있다”고 말했다.
이어 “신청 전 서류 관련 준비 절차는 이미 진행 중”이라고 덧붙였다.
큐비스 조인트는 CT영상을 기반으로 수술 전 수립한 수술계획에 따라 뼈는 절삭하는 관절 수술 로봇이다. 핵심은 관절 수술의 성공도를 높이는 역할을 하며 의료진은 큐비스 조인트를 사용, 다양한 절삭 옵션을 사용한다. 대표적으로 선택부위별 자동절삭(밀링), 드릴링 가이드 등 뼈 절삭 및 보조 기능과 비상시 절상중지기능, 절삭 툴 후퇴 기능이 있어 안정성이 높은 것으로 알려졌다. 수술의 실시간 체크도 가능하다.
또한 OTS(Optical Tracking System)를 이용한 정합방식으로 사용자 편의성을 향상하고 컴팩트한 디자인으로 수술실 설치 공간을 최소화했다. 6축 수직 다관절(Robot Arm)을 이용해 더 넓은 수술 영역을 제공하며 오픈 플랫폼으로 다양한 임플란트 사용도 가능하다.
앞으로 핵심 전략은 수출국 확대다. 큐렉소는 현재 국내를 비롯해 인도 시장에 수출하고 있으며 유럽 판매를 위한 CE 인증(2020년 9월 서류 제출 및 심사 중) 절차를 밟고 있다. 내부에선 자체 개발 수술 로봇을 KFDA, CE, FDA 순으로 인허가를 추진하는 전략을 짜고 있으며 아시아에서 출발해 유럽, 호주, 미국 등 선진국으로 진출하는 것을 핵심으로 한다.
미국 FDA 신고 절차가 접수 후 90일 이내에 검토 완료 과정을 거치는 만큼 내년 1분기가 허가 시점으로 점쳐지고 있다.