조건부 허가 권고했지만 일부 제한된 환자군에 사용해야
식품의약품안전처 법정 자문기구인 중앙약사심의위원회가 셀트리온의 신종 코로나바이러스 감염증(코로나19) 치료제 ‘렉키로나주’에 대해 조건부 허가 의견을 내놨다.
중앙약사심의윈회는 27일 셀트리온의 항체치료제 ‘렉키로나주960mg(레그단비맙)’의 안전성과 효과 등에 대해 자문한 결과 3상 임상시험 결과를 시판 후 제출하는 것을 조건으로 조건부 허가를 권고했다.
다만 검증 자문단 의견과 달리 경증 환자에게 렉키로나주를 투약하는 것의 임상적 의미는 결론내리기 어렵고, 중등증 환자와 고위험군 경증 환자 등 일부 제한된 환자군에서 사용할 것을 권고했다.
이동희 식품의약품안전평가원장은 "임상 2상에 대한 임상시험 결과를 종합적으로 고려했을 때 경증환자에 대해서는 처음 임상시험 시작할 당시의 통계적 검증 방법들이 정립돼 있지 않은 상태였고, 임상 2상 단계에서 충분한 환자 수를 확보하지 못해 경증환자에서는 통계적으로 유의할 정도의 치료효과를 확인하지 못했다"며 "경증환자가 중증으로 이환하는 것을 예방하는 효과가 있는지에 대한 최종 결론은 3상 임상시험 결과를 본 후에 결정하기로 했다"라고 말했다.
제한된 환자군에 사용할 것을 권고하면서도 조건부 허가 의견을 낸 이유에 대해선 의료진의 선택권을 보장하기 위한 것이라고 설명했다. 이 원장은 "국가적인 위험과 팬데믹한 상황에서 의료진들이 경증환자라 할지라도 고위험군에 처해 있는, 코로나로 아주 심각한 부작용이 예상되는 그런 경우에 의료진들이 사용할 수 있는 선택권을 최대한 존중하기 위해서"라고 말했다.
중앙약사심의위원회는 렉키로나주 투여 후 안전성과 관련해 업체가 제출한 자료를 바탕으로 현재 수준에서 생명을 위협하는 중대한 이상사례는 발생하지 않았지만, 충분한 환자 수를 대상으로 3상 임상시험과 시판 후 지속적인 안전성 평가가 필요하다고 강조했다. 아울러 일부 위원들의 경우 소수의견으로 의약품 품목허가보다는 특례 제조 승인 등을 활용하는 것을 제안했다.
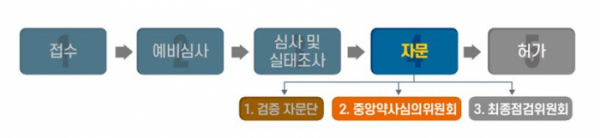
식약처는 셀트리온 렉키로나주와 관련한 품질자료 일부 등 심사자료를 제출받아 검토를 진행하고 ‘코로나19 치료제 안전성·효과성 검증 자문단’과 이번 ‘중앙약사심의위원회’ 자문을 통해 얻은 전문가 의견, 효능·효과, 권고사항 등을 종합해 ‘최종점검위원회’를 통해 ‘렉키로나주’의 허가 여부를 최종 결정할 예정이다.





