금융감독원이 제약·바이오 업종의 개발비 회계처리 부분을 집중 감리하면서 투자심리가 크게 위축된 상황이다. 하지만 실제 규제는 우려보다 느슨할 전망이다. 임상 3상 이상에 대해서만 개발비 자산화를 허용할 것이라는 예측과 달리 국내 기업 현실에 맞게 케이스별로 검토한다는 방침이다.
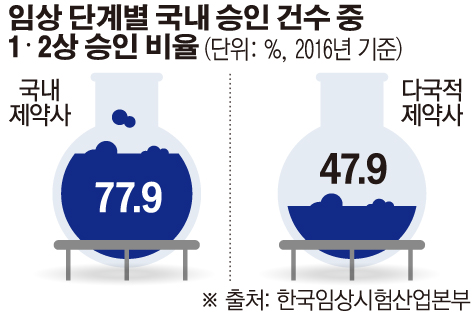
21일 금감원의 ‘제약·바이오 업종의 개발비 회계처리 신뢰성 제고방안’ 중 한국임상시험산업본부에서 가져온 통계에 따르면 2016년 기준 국내 제약·바이오 기업의 연구는 임상 1상과 2상에 77.9% 가량 몰려있다. 다국적 제약사의 경우 임상 단계별 승인 건수 중 1·2상 비율이 47.9%인 것과 비교하면 현저히 높은 수준이다.
국내 기업 대부분이 신약 후보 물질 개발에 연구·개발(R&D)을 집중하고 다국적 제약사에 기술을 수출하는 방식으로 수익을 내는 것으로 해석할 수 있다.
금감원이 개발비 회계처리 부분을 들여다보기 시작한 것은 IFRS를 채택한 타국의 사례와 개발비 인식 관련 균형이 맞지 않는다는 판단에서다. 특히 올해 집중 감리에 나선 것은 제재가 강화된 새 외부감사법이 2018사업연도 재무제표부터 적용되기 때문이다. 기업들이 이번 사업연도 재무제표를 내년에 공시했을 때 분식회계가 적발될 경우 분식 금액의 최대 20%까지 과징금이 부과될 수 있다.
IFRS를 전면 도입한 독일, 영국, 프랑스, 덴마크, 호주 등 5개 국가의 8개 글로벌 제약사의 경우 개발비 자산화 시점을 ‘정부 승인’이 난 때로 잡고 있다. 미국 내 13개 제약사도 개발 원가를 비용 처리하고 있다.
반면 국내에서 개발비 자산화 정책을 공시한 115개 제약·바이오사 중 자산화 기준을 구체적으로 제시한 곳은 30곳에 불과했다. 자산화 시점이 3상 이하(전임상 1·2·3상) 단계인 경우가 23곳에 달했다.
금감원은 개발비의 자산화 시점과 관련해 외국 사례와 같은 엄격한 기준을 일률적으로 적용하지는 않을 방침이다. 국내 회사들이 글로벌 제약사에 비해 여러 가지 방식으로 수익을 내고 있어 개발비의 자산화를 판단하는 시점이 제각각 다를 수 있다는 판단 때문이다.
또 국내 승인이나 판매허가를 얻은 제품이 해외 승인을 얻기 위해 현지에서 다시 임상시험을 진행하는 경우 예외적으로 낮은 임상단계에서도 개발비 자산화가 가능할 것으로 전망된다. 다만 등록 가능성이 매우 높고 현지 허가장벽이 낮아 임상 시험이 사실상 형식적인 경우 등에 한한다.
반면 개발 진행 중인 치료제가 임상 단계에서 내용이 변경되는 경우에는 약효가 동일하더라도 요건에 따라 임상을 새로 진행해야 하므로 사업의 연속성 판단을 엄격히 해야 한다. 개발 중인 사업에 대한 잠정적인 평가를 바탕으로 중장기 사업계획을 작성하는 것 역시 자산화하기에는 적절치 못한 것으로 제시됐다.
금감원 관계자는 “이번 집중감리는 감독당국이 기업들을 규제하려는 것이 아니다”라며 “신중한 회계처리를 유도하면서 산업의 성장성을 제한하지 않는 차원에서 회계기준을 제시하려는 것”이라고 말했다.