한미 1호 신약 ‘올리타’ 생산 중단…임상시험 장기화에 시장진입 늦고 처방약 리스트 등재 기회도 적어…업계 “우선 입찰제도 등 지원 필요”
한미약품의 올리타 개발 중단은 국내 제약·바이오 업계에 시사하는 바가 적지 않다. 해외 공룡 제약사들이 세계 시장을 선점하고 있는 상황에서 국내 업체가 글로벌 신약을 개발해 상용화에 성공하기가 얼마나 어려운지를 새삼 일깨우는 계기가 됐다는 분석이 많다. 또 국산 신약이 단순히 출시됐다는 점에 의미를 부여할 것이 아니라 시장 경쟁력을 갖추기 위한 전략을 함께 고민해야 한다는 교훈도 남겼다.
업계에서는 올리타의 운명이 이미 예고됐다는 분석이 지배적이다. 800억 원을 주고 올리타 개발 기술을 도입한 베링거인겔하임사는 2016년 9월 개발권 도입 포기를 알려왔다. 이는 동일한 환자에게 사용하는 글로벌 경쟁 약물인 아스트라제네카의 ‘타그리소’가 이미 기술 이전을 마친 2015년 같은 해 미국 등 40여 개국에서 판매 허가를 받으면서 글로벌 시장에서 경쟁력을 잃은 것이 결정적인 계기가 됐다. 베링거인겔하임으로서는 이미 경쟁 약물이 허가를 받고 시장을 빠르게 점유해 나가는 상황에서 임상시험에 수천억 원을 추가로 쏟아부을 이유가 없었던 것이다. 특히 지난달 29일엔 중국의 파트너사였던 자이랩사도 올리타의 임상 3상이 늦어진다는 이유로 올리타의 도입을 포기하면서 가장 큰 시장인 중국에서의 임상 3상 진행이 불투명해졌다. 한미약품 측은 “불굴의 의지로 올리타를 개발하려 했으나 향후 개발에 투입될 연구( R&D) 비용 대비 신약 가치의 현저한 하락이 확실하다는 판단에 따라 개발 중단을 결정했다”고 밝혔다.
이번 사례에서 볼 수 있듯 국산 신약은 비교적 늦게 개발돼 이미 성숙한 시장에 진입하는 경우가 많다. 이 때문에 출시되더라도 후발주자인 국내 개발신약의 경우 글로벌 제약사들의 선발 약제들에 밀려 대형 병원 처방 리스트에 등재될 기회가 제한될 수 있다. 더 큰 문제는 내수 시장에서의 임상 데이터나 사용 경험 부족으로 이어져 적응증 확대를 위한 임상시험이 장기화되면서 글로벌 시장 진입 자체가 늦어진다는 점이다.
실제 식품의약품안전처에 따르면 1999년 우리나라에서 처음으로 신약이 개발된 후 18년이 지난 지난해 말까지 국내에서 개발된 신약은 29개에 불과하다. 이 중에서도 연간 100억 원 이상의 매출을 올린 블록버스터급 제품은 보령제약의 고혈압치료제 ‘카나브’, LG화학의 당뇨병치료제 ‘제미글로’, 일양약품의 항궤양제 ‘놀텍’ 등 3개뿐이다. 힘들게 신약을 개발했더라도 효능이나 마케팅에서 경쟁력을 갖추지 못하면 안방에서조차 기를 펴지 못한다는 것을 보여주는 대목이다.
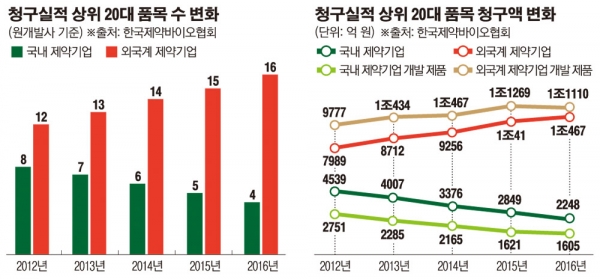
한국제약바이오협회가 2012~2016년 최근 5년간 국내 제약사의 처방약 품목과 건강보험 청구액, 청구비중을 분석한 결과에서도 이 같은 현실은 여실히 드러난다. 상위 100대 품목 중 국내 제약사 제품의 개수는 2012년 43개에서 2016년 41개로 줄었다. 상위 20대 처방약 품목 중에서는 같은 기간 8개에서 4개로 반 토막이 났다. 2013년부터 2016년까지 청구 실적 상위 20대 품목에 신규 진입한 품목은 6개로, 모두 외국계 제약기업 제품이었다.
청구액 비중도 감소세다. 상위 20대 품목 중 국내 제약기업 제품의 청구액은 2012년 4539억 원에서 2016년 2248억 원으로 5년 사이 절반으로 감소했다. 상위 100대 품목에서는 전체 약품비 청구액은 2012년 3조1707억 원, 2016년 3조3039억 원인데 이 가운데 국내 제약사 비중은 이 기간 41.1%에서 34.4%로 낮아졌다. 그마저도 상위 100대 품목에 있는 국내사 개발품목 그룹 중 청구비중이 가장 큰 그룹은 개량신약으로 2012년 8품목에서 2016년 12품목으로 증가했다.
협회는 국내 제약기업 제품의 시장점유율이 감소한 원인을 최근 5년간 다국적 제약사가 고가의 신약을 대형 품목으로 빠르게 키워내며 건강보험 시장에 활발하게 진입시켰기 때문으로 봤다. 또 국내 제약사들이 신약과 개량신약 등을 대형 품목으로 성장시키지 못한 것도 원인으로 지목했다.
그러면서 글로벌 신약 개발 경쟁이 치열해지는 가운데 토종 신약들이 경쟁력을 갖추기 위해선 정부의 지원이 필요하다고 제언했다. 협회 관계자는 “공공의료기관 처방약 목록에 국산 신약을 의무 등재하거나 우선 입찰할 수 있는 제도를 운영해야 한다”며 “정부가 의료기관의 국산 신약 사용실적을 평가지표나 지원정책 가점 요소에 반영한다면 국내 제약사가 실제 의료현장에 진입하는 기간을 크게 단축시킬 수 있을 것으로 기대된다”고 말했다.